A Anvisa (Agência Nacional de Vigilância Sanitária) determinou, por meio da Resolução nº 641 publicada na quarta-feira (18), a apreensão, proibição e, em alguns casos, o recolhimento de remédios utilizados no tratamento de câncer, diabetes e hipertensão por estarem em em desacordo com a regulamentação.
Entre os produtos atingidos pela medida está o lote 416466 do medicamento Enhertu (trastuzumabe deruxtecana), indicado para cânceres HER2-positivo e HER2-baixo, como mama, gástrico e pulmão. A ação prevê apreensão e proibição de comercialização e distribuição.
De acordo com a Anvisa, a própria empresa Daiichi Sankyo Brasil Farmacêutica Ltda. comunicou a identificação, no mercado, de unidades do lote com características divergentes do padrão original.
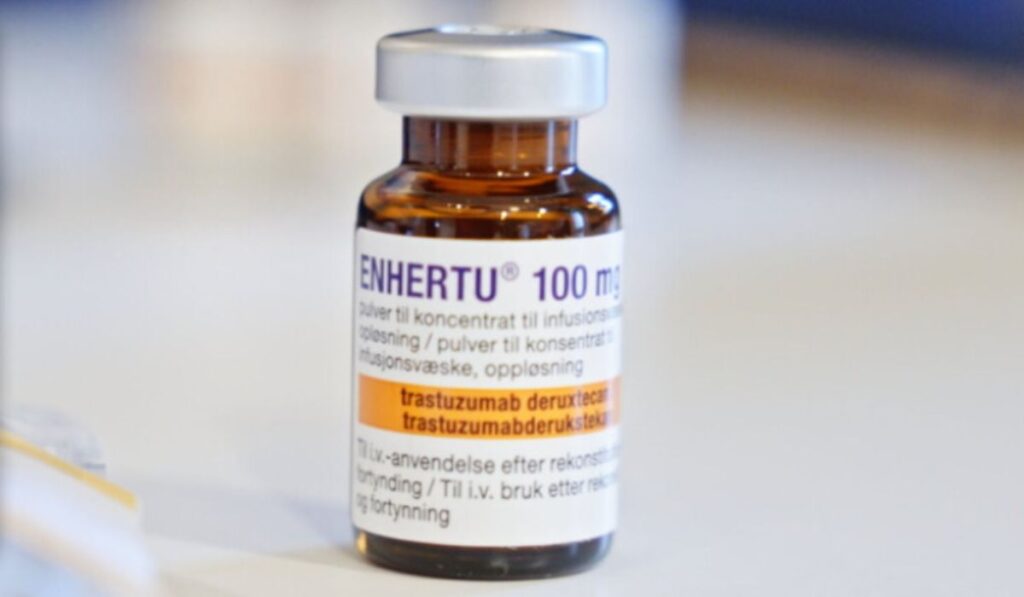
Foto: Divulgação/Conselho Federal da Farmácia/ND Mais
Foram relatados frascos com dimensões superiores às habituais, descascamento na tampa e alteração no material e na coloração, enquanto o original possui tampa amarela de aparência plástica, algumas unidades apresentavam tampa metálica pintada de amarelo. A suspeita é de possível falsificação ou desvio na cadeia de distribuição.
Anvisa proibiu remédios, dentre eles um semelhante ao Mounjaro, e recolheu lotes de anti-hipertensivo
Outro alvo da resolução é o Tizerc, medicamento injetável (semelhante ao Mounjaro), indicado para diabetes tipo 2, obesidade e emagrecimento. A Anvisa determinou a apreensão de todos os lotes, proibição de armazenamento, comercialização, distribuição, importação, propaganda, transporte e uso do produto fabricado pela empresa Quimfa S/A.
Segundo o órgão regulador, houve comprovação de propaganda e anúncio de venda do medicamento sem registro na Anvisa. Além disso, a fabricante não possui Autorização de Funcionamento para produzir medicamentos e, conforme inspeção sanitária, não cumpre as boas práticas de fabricação exigidas pela legislação brasileira
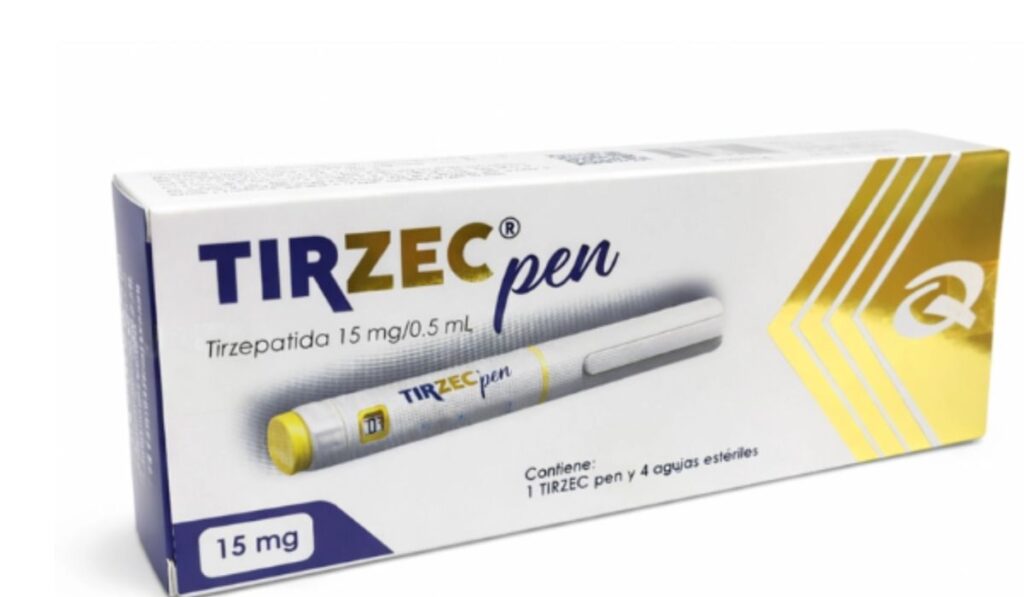
Foto: Divulgação/Columbia Farmácia/ND Mais
Já no caso do maleato de enalapril 20 mg (apresentação com 500 comprimidos), utilizado no tratamento da hipertensão e insuficiência cardíaca, a medida foi de recolhimento voluntário dos lotes 2427112, 2427068, 2427108 e 2427111. O recolhimento foi iniciado pela própria empresa após a detecção de manchas nos comprimidos, atribuídas ao lubrificante de grau alimentício utilizado no processo de compressão.
Embora análises tenham confirmado ausência de risco ao paciente, a irregularidade fere o artigo 4º da RDC nº 658/2022, por caracterizar produção e comercialização em desacordo com o registro sanitário e com as boas práticas de fabricação.
A Anvisa proibiu remédios e orienta que pacientes que utilizam os medicamentos afetados verifiquem o número do lote nas embalagens e procurem orientação médica ou farmacêutica em caso de dúvidas. Denúncias sobre comercialização irregular podem ser feitas pelos canais oficiais da agência.
Por: ND Mais






